Una mappa del tessuto umano adiposo bianco ottenuta integrando dati di transcrittomica (espressione genica) da singola cellula e da sezioni tissutali.

Contributo di Gabriella Milan
Una mappa del tessuto umano adiposo bianco ottenuta integrando dati di transcrittomica (espressione genica) da singola cellula e da sezioni tissutali.
Abstract: Fino ad ora gli studi sul tessuto adiposo (TA) bianco umano a livello di analisi su singola cellula sono stati condotti utilizzando piccoli gruppi di soggetti e non vi è accordo condiviso sulla nomenclatura delle popolazioni cellulari identificate. In questo studio abbiamo realizzato una meta-analisi comprensiva dei dati disponibili in letteratura e generati da noi mediante analisi dei trascritti (mRNA) su singola cellula, su singolo nucleo e di transcrittomica spaziale a partire da TA bianco umano di 3 diversi depositi adiposi: sottocutaneo, omentale e perivascolare. La mappa ad alta risoluzione del TA bianco è stata ottenuta dai dati di 10 studi indipendenti e ci ha permesso di identificare più di 60 sottopopolazioni diverse appartenenti a tipi cellulari distinti quali cellule immunitarie, cellule vascolari, fibroblasti e progenitori adipogenici e adipociti maturi, sulla base dei trascritti specifici da loro espressi. A partire da questi risultati abbiamo analizzato ulteriormente i dati di espressione provenienti da esperimenti di trascrittomica spaziale (a partire da sezioni tissutali, mantenendo la topografia del tessuto e i rapporti topografici tra le cellule della sezione) e di analisi di espressione su tessuto intero (provenienti da ulteriori 9 coorti di soggetti) al fine di aggiungere dettagli relativi alla localizzazione spaziale, ai rapporti di vicinanza tra le cellule e alle caratteristiche cliniche dei soggetti. Questa analisi ci ha permesso di ottenere informazioni sulle interazioni tra cellula e cellula all’interno del tessuto e sulle relazioni tra specifici tipi cellulari e insulino-resistenza, dislipidemia, volume dell’adipocita, attività lipolitica e cambiamenti del peso corporeo a lungo termine (2 e 5 anni dopo chirurgia bariatrica). Nel suo complesso la meta-mappa che abbiamo realizzato rappresenta una ricca risorsa che descrive il TA bianco a livello della sua composizione cellulare e della sua architettura e suggerisce una possibile associazione tra specifici tipi cellulari e fenotipi metabolici clinici.
Commento: Le nuove tecnologie basate sul sequenziamento massivo offrono la possibilità di raccogliere e confrontare mediante tecniche informatiche e statistiche avanzate un enorme quantità di informazioni. Questo lavoro raccoglie e confronta dati relativi all’espressione genica del TA bianco umano ottenuti analizzando nuovi campioni e dati pubblicati, disponibili pubblicamente. L’approccio bioinformatico e i diversi software utilizzati per l’analisi sembrano adeguati e tengono conto della recente letteratura sull’argomento che comincia anche ad evidenziare i problemi e i limiti di queste tecnologie, sicuramente potentissime ma spesso difficili da gestire e da interpretare. Teniamo sempre conto poi che l’analisi dei trascritti (trascrittomica) è una fotografia dei geni che in quel preciso momento vengono espressi da una singola cellula, nel caso di sequenziamento di RNA a livello di singola cellula o single-cell RNA sequencing (scSeq), o sono presenti nel nucleo di una singola cellula, nel caso di sequenziamento di RNA a livello di singolo nucleo o single-nucleus RNA sequencing (snSeq). Quindi tali dati non danno nessuna informazione sulla presenza delle relative proteine codificate da quei trascritti né sulla funzione che le stesse esercitano nella cellula in cui eventualmente vengano prodotte. L’enorme quantità di dati analizzati (401.302 cells/nuclei, indicati come oggetti in Figura 1, pannello a) è stata ottenuta nel suo complesso da 103 campioni provenienti da 83 soggetti con età e BMI estremamente variabili. Possiamo intuire quindi la complessità di analizzare e soprattutto unire dati provenienti da coorti molto differenti e generati con metodiche diverse, ciascuna con limiti e peculiarità. Da qui l’importanza di conoscere e utilizzare software informatici adeguati, corrette procedure statistiche e di seguire strade decisionali precise su come unire e interpretare i risultati.
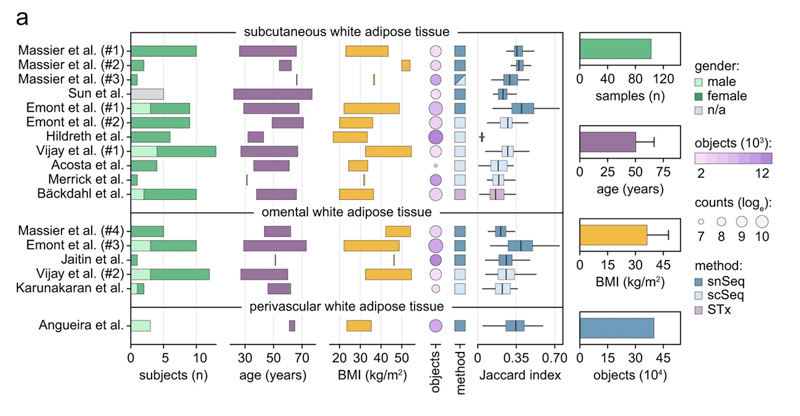
Figura 1, pannello a. Caratteristiche principali dei campioni analizzati nel presente studio (Massier at al.#1-4) e da studi precedentemente pubblicati, con l’indicazione del numero, età e BMI dei soggetti da cui sono stati ottenuti e del metodo molecolare utilizzato.
Riassumo brevemente le conclusioni generali di impatto fisiopatologico e clinico che i dati analizzati in questo lavoro suggeriscono, ricordando che esso è ricchissimo di informazioni che costituiranno la base per tantissimi studi futuri e senza addentrarmi in tecnicismi per addetti ai lavori.
- I principali tipi cellulari presenti nel TA bianco umano sono: i fibroblasti e precursori adipogenici (detti FAPs) che rappresentano la classe più rappresentata (circa 40%), gli adipociti maturi e le cellule del sistema immune che sono presenti in rapporto 1:1 (circa 20% ciascuno) e le cellule vascolari (circa 15%).Teniamo presente che questa composizione riflette le procedure di dissociazione del TA a sospensione a singola cellula, che certamente determinano la perdita di adipociti maturi, e del fatto che la componente di cellule immunitarie proviene anche dai vasi che irrorano il tessuto. Pertanto questa composizione riflette maggiormente la composizione della frazione vasculo-stromale piuttosto che quella del TA, anche se i dati generati in questa prima parte verranno poi integrati con dati ottenuti su sezioni (trascrittomica spaziale) e su RNA estratto da TA intero non dissociato (bulk trascriptomic data).
- Il primo dato interessante è che la comparazione dei diversi depositi adiposi (sottocutaneo, omentale e perivascolare) non mette in evidenza differenze significative tra l’abbondanza dei diversi tipi cellulari.
- Le cellule immunitarie presenti in maggiore quantità sono i monociti, i macrofagi e le cellule dendritiche (che nel loro insieme rappresentano il 67%), poi le cellule T, Natural Killer (NK) e NKT (29%), molto minori i mastociti (3%), i linfociti B (1%) e le plasmacellule (0,2%). Per quanto riguarda le cellule mieloidi è possibile identificare, in base ai trascritti, svariati tipi di gruppi che includono macrofagi, monociti classici e non classici, differenti sottopopolazioni M2, vari tipi M1, in particolare i macrofagi associati ai lipidi (LAM), i macrofagi regolati metabolicamente (MMe), i macrofagi redox regolatori metabolici (Mox), e infine gruppi M1/M2 misti.
- Considerando il profilo di espressione delle cellule dei vasi si possono identificare sia cellule che stimolano sia cellule che inibiscono la vascolarizzazione e si individuano cellule che potrebbero rappresentare uno stato intermedio di transizione tra cellula endoteliale e precursore adipogenico.
- Nella classe dei FAPs è possibile identificare sottopopolazioni con differente livello di differenziamento in senso adipogenico; il marcatore CD34 risulta espresso da molte di queste. Tra i depositi adiposi (sottocutaneo e omentale) si osserva un buon grado di sovrapposizione anche se esistono dei marcatori espressi in modo deposito-specifico. Alcune sottopopolazioni identificate nel topo non si ritrovano nel TA umano.
- I dati sugli adipociti maturi risultano più inconsistenti ed evidenziano un grado di eterogeneità cellulare minore che non sembra suggerire la presenza di sottopopolazioni differenti di adipociti maturi.
- Le analisi di relazione tra i tipi cellulari basate sull’espressione di ligandi e recettori evidenziano una segnalazione preferenziale tra FAPs e macrofagi di tipo M2.
- Le analisi di distribuzione spaziale (basate su un numero minore di dati e su di un unico lavoro) suggeriscono il contatto tra sottopopolazioni di FAPs e cellule endoteliali e di altre sottopopolazioni di FAPs con LAMs, suggerendo la presenza di differenti nicchie adipogeniche nel TA.
- L’analisi dei dati di espressione in relazione ai dati clinici rappresenta una conferma di dati molto ben assodati nella letteratura. Vengono identificati 3 gruppi di tipi cellulari: il cluster A che associa positivamente con un profilo metabolico migliore (contenente 6 tipi cellulari ciascuno identificato da uno specifico profilo di espressione), il cluster B (contenente 15 tipi cellulari) che correla negativamente con gli stessi parametri e il cluster C (contenente 37 tipi cellulari) che non mostra nessuna associazione significativa con il fenotipo metabolico dei soggetti. Da rilevare che in queste analisi l’età dei soggetti NON risulta correlata a nessun tipo cellulare. Il cluster B è rappresentato per la maggior parte da cellule del sistema immunitario, confermando che la flogosi rappresenta il determinante più importante per uno stato di obesità e di insulino-resistenza. Il Cluster A invece è rappresentato da cellule vascolari (capillari endoteliali), indicando come la vascolarizzazione sia importante per il mantenimento di un TA sano. Per quanto riguarda i FAPs, nel cluster A sono contenuti i precursori adipogenici in stadi di differenziamento intermedio e avanzato, mentre nel cluster B è contenuto il gruppo di precursori individuato dagli autori come quello più indifferenziato (CD55+) da cui potrebbero originare tutti gli altri. Questi dati sembrerebbero suggerire che il differenziamento adipogenico possa essere regolato sia positivamente che negativamente in corso di obesità e di alterazioni metaboliche.
- Infine nelle meta-analisi realizzate su coorti di pazienti sottoposti a chirurgia bariatrica e analizzati dopo 2/5 anni dall’intervento tutte le diverse popolazioni cellulari vengono normalizzate dal calo ponderale eccetto le cellule endoteliali capillari, suggerendo che la rarefazione di capillari che si osserva in corso di obesità costituisca una perdita non reversibile. Questi risultati sembrerebbero indicare che la composizione del TA bianco umano sia dinamica e si modifichi con la variazione della massa grassa.
Ricordo infine che nel prossimo Congresso Europeo dell’Obesità che si terrà a Venezia (12-15 maggio 2024) organizzato con la collaborazione della SIO, avrà luogo una sessione tecnologica nella quale si parlerà appunto di come queste e altre tecnologie innovative possano contribuire a definire in modo sempre più preciso i fenotipi differenti dei pazienti con obesità e di come si potranno trasformare da strumenti di ricerca tecnologica di nicchia in test diagnostico-clinici per la gestione pratica dei pazienti.
Altri lavori interessanti:
- Bäckdahl J, Franzén L, Massier L, Li Q, Jalkanen J, Gao H, Andersson A, Bhalla N, Thorell A, Rydén M, Ståhl PL, Mejhert N. Spatial mapping reveals human adipocyte subpopulations with distinct sensitivities to insulin. Cell Metab. 2021 Sep 7;33(9):1869-1882.e6. doi: 10.1016/j.cmet.2021.07.018.
- Emont MP, Jacobs C, Essene AL, Pant D, Tenen D, Colleluori G, Di Vincenzo A, Jørgensen AM, Dashti H, Stefek A, McGonagle E, Strobel S, Laber S, Agrawal S, Westcott GP, Kar A, Veregge ML, Gulko A, Srinivasan H, Kramer Z, De Filippis E, Merkel E, Ducie J, Boyd CG, Gourash W, Courcoulas A, Lin SJ, Lee BT, Morris D, Tobias A, Khera AV, Claussnitzer M, Pers TH, Giordano A, Ashenberg O, Regev A, Tsai LT, Rosen ED. A single-cell atlas of human and mouse white adipose tissue. Nature. 2022 Mar;603(7903):926-933. doi: 10.1038/s41586-022-04518-2.
- Norreen-Thorsen M, Struck EC, Öling S, Zwahlen M, Von Feilitzen K, Odeberg J, Lindskog C, Pontén F, Uhlén M, Dusart PJ, Butler LM. A human adipose tissue cell-type transcriptome atlas. Cell Rep. 2022 Jul 12;40(2):111046. doi: 10.1016/j.celrep.2022.111046.
An integrated single cell and spatial transcriptomic map of human white adipose tissue. Massier L, Jalkanen J, Elmastas M, Zhong J, Wang T, Nono Nankam PA, Frendo-Cumbo S, Bäckdahl J, Subramanian N, Sekine T, Kerr AG, Tseng BTP, Laurencikiene J, Buggert M, Lourda M, Kublickiene K, Bhalla N, Andersson A, Valsesia A, Astrup A, Blaak EE, Ståhl PL, Viguerie N, Langin D, Wolfrum C, Blüher M, Rydén M, Mejhert N.
Nat Commun. 2023 Mar 15;14(1):1438. doi: 10.1038/s41467-023-36983-2.