Orforglipron: agonista orale giornaliero del recettore GLP-1 in soggetti adulti obesi

Contributo: Del Prete
Orforglipron: agonista orale giornaliero del recettore GLP-1 in soggetti adulti obesi
Orforglipron: agonista orale giornaliero del recettore GLP-1 in soggetti adulti obesi
Background:
L’obesità è un importante fattore di rischio per molte delle principali cause di malattia e di morte in tutto il mondo. Gli agonisti recettoriali del GLP-1 (GLP-1AR) sono farmaci a base peptidica somministrati tramite iniezioni sottocutanee. Attualmente, semaglutide è l’unico GLP-1RA orale approvato per il trattamento del diabete mellito di tipo 2 (DM2). Orfoglipron è un nuovo agonista del recettore non peptidico del peptide-1 (GLP-1) per cui sono necessari dati riguardanti l’efficacia e la sicurezza come terapia orale una volta al giorno per la riduzione del peso negli adulti con obesità.
Obiettivi:
Valutare l’efficacia e la sicurezza della somministrazione orale giornaliera di orforglipron in adulti non diabetici obesi o con sovrappeso.
Metodi:
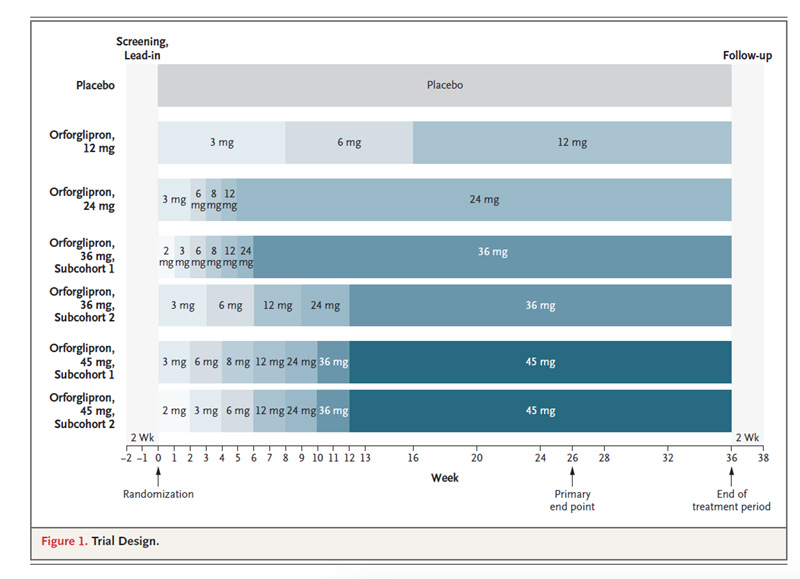
In questo studio di fase 2, randomizzato, in doppio cieco, sono stati arruolati adulti con obesità o con sovrappeso più almeno una condizione coesistente correlata al peso e senza diabete. I partecipanti sono stati assegnati in modo casuale a ricevere orforglipron in una delle quattro dosi (12, 24, 36 o 45 mg) o placebo una volta al giorno per 36 settimane (Figura 1). La variazione percentuale rispetto al basale del peso corporeo è stata valutata alla settimana 26 (endpoint primario) e alla settimana 36 (endpoint secondario).
Risultati:
Un totale di 272 partecipanti è stato sottoposto a randomizzazione. Al basale, il peso corporeo medio era di 108,7 kg e l’indice di massa corporea medio (Kg/m2) era 37,9. Alla settimana 26, la variazione media del peso corporeo rispetto al basale variava da -8,6% a -12,6% nelle coorti trattate con orforglipron ed era -2,0% nel gruppo placebo (Figura 2). Alla settimana 36, la variazione media variava da -9,4% a -14,7% con orforglipron ed era -2,3% con placebo (Figura 2). Una riduzione di peso di almeno il 10% entro la settimana 36 si è verificata nel 46-75% dei casi, nei partecipanti che hanno ricevuto orforglipron, rispetto al 9% che ha ricevuto il placebo. L’uso di orforglipron ha portato a un miglioramento di tutti i parametri cardiometabolici e le condizioni correlate al peso prespecificate (ipertensione, dislipidemia, malattie cardiovascolari o sindrome ostruttiva delle apnee notturne). Gli eventi avversi più comuni riportati con orforglipron sono stati eventi gastrointestinali, di entità da lieve a moderata e principalmente durante l’incremento della dose, e ha portato all’interruzione di orforglipron nel 10-17% dei partecipanti nelle coorti di dosaggio. Il profilo di sicurezza di orforglipron è risultato coerente con quello della classe degli agonisti del recettore GLP-1.
Conclusioni:
L’orforglipron, agonista non peptidico del recettore del GLP-1 orale giornaliero, è stato associato a riduzione del peso. Gli eventi avversi riportati con orforglipron risultano simili a quelli riscontrati con gli agonisti iniettabili del recettore del GLP-1. (Finanziato da Eli Lilly; numero GZGI ClinicalTrials.gov, NCT05051579.)
Commento:
I GLP-1AR sono un’opzione terapeutica consolidata per il DM2 e il controllo cronico del peso, con un profilo di sicurezza comprovato [1]. I GLP-1AR sono farmaci a base peptidica che richiedono iniezioni sottocutanee. Attualmente, l’unico GLP-1RA orale approvato è una formulazione di semaglutide in compresse che, per essere assorbita, richiede di essere miscelata con un potenziatore dell’assorbimento gastrico: il salcaprozato di sodio [2]. La compressa deve essere assunta a stomaco vuoto, almeno 30 minuti prima di mangiare o bere o assumere altri medicinali orali, e con non più di 120 ml di acqua [3]. Nonostante queste accortezze, la formulazione orale di semalutide ha una biodisponibilità compresa tra appena lo 0,4% e l’1,0% [4].
Orforglipron appartiene a una nuova classe di GLP-1RA non peptidici orali, sintetizzati chimicamente. Orforglipron è un potente agonista parziale del recettore GLP-1 che, grazie una maggiore attivazione della via dell’AMPciclico (cAMP) rispetto al reclutamento della β-arrestina, potrebbe offrire una una desensibilizzazione recettoriale inferiore rispetto agli agonisti completi del recettore GLP-1 [5]. Orforglipron, essendo una molecola non proteica non prevede restrizioni sulla somministrazione di cibo o acqua [6].
Lo studio di fase 2, di Wharton et al., ha stimato l’efficacia di schemi di dosaggio multipli di orforglipron rispetto al placebo, a 26 e 36 settimane, in adulti non diabetici, con obesità o con sovrappeso più almeno una comorbilità correlata al peso. Lo studio ha mostrato una riduzione dose-dipendente del peso corporeo e dell’indice di massa corporea che, a 36 settimane, non aveva ancora raggiunto il plateau; ciò è coerente con gli studi con altri GLP-1RA che hanno mostrato una perdita di peso fino a 60 settimane. Il calo ponderale sembrerebbe essere superiore a liraglutide e ai farmaci orali non incretinici naltrexone-bupropione e fentermina-topiramato, sarebbe in linea con semaglutide 2,4 mg sottocutanea [7] e semaglutide 50 mg orale [8], mentre risulterebbe inferiore alle dosi maggiori di tirzepatide [7].
Secondo gli Autori, gli eventi avversi e i drop out sarebbero in linea con gli studi di fase 2 degli altri GLP-1AR [9].
Anche se probabilmente inferiore a tirzepatide, orforglipron si è dimostrato promettente per la perdita di peso, in quanto sembra almeno paragonabile a semaglutide. Se gli studi di fase 3 confermeranno i dati di efficacia e sicurezza di ortoglifon, potremmo avere un farmaco per il trattamento dell’obesità che presenterà l’indubbio vantaggio di una somministrazione orale svincolata dall’alimentazione.
Bibliografia
- Lincoff AM, Brown-Frandsen K, Colhoun HM, et al. Semaglutide and Cardiovascular Outcomes in Obesity without Diabetes. N Engl J Med. 2023 Dec 14;389(24):2221-2232. doi: 10.1056/NEJMoa2307563. Epub 2023 Nov 11.
- Kim JC, Park EJ, Na DH. Gastrointestinal Permeation Enhancers for the Development of Oral Peptide Pharmaceuticals. Pharmaceuticals (Basel). 2022 Dec 19;15(12):1585. doi: 10.3390/ph15121585.
- European Medicines Agency. Rybelsus-INN semaglutide. Riassunto delle caratteristiche del prodotto. https://ec.europa.eu/health/documents/community-register/2022/20221216157986/anx_157986_it.pdf (ultima visita: 17/12/2023).
- Granhall C, Donsmark M, Blicher TM, et al. Safety and Pharmacokinetics of Single and Multiple Ascending Doses of the Novel Oral Human GLP-1 Analogue, Oral Semaglutide, in Healthy Subjects and Subjects with Type 2 Diabetes. Clin Pharmacokinet. 2019 Jun;58(6):781-791.
doi: 10.1007/s40262-018-0728-4.
- Kawai T, Sun B, Yoshino H, et al. Structural basis for GLP-1 receptor activation by LY3502970, an orally active nonpeptide agonist. Proc Natl Acad Sci U S A. 2020 Nov 24;117(47):29959-29967. doi: 10.1073/pnas.2014879117. Epub 2020 Nov 11.
- Pratt E, Ma X, Liu R, Robins D, et al. Orforglipron (LY3502970), a novel, oral non-peptide glucagon-like peptide-1 receptor agonist: A Phase 1b, multicentre, blinded, placebo-controlled, randomized, multiple-ascending-dose study in people with type 2 diabetes. Diabetes Obes Metab. 2023 Sep;25(9):2642-2649. doi: 10.1111/dom.15150. Epub 2023 Jun 1.
- Chakhtoura M, Haber R, Ghezzawi M, et al. Pharmacotherapy of obesity: an update on the available medications and drugs under investigation. EclinicalMedicine. 2023 Mar 20:58:101882. doi: 10.1016/j.eclinm.2023.101882. eCollection 2023 Apr.
- Knop FK, Aroda VR, do Vale RD, et al. Oral semaglutide 50 mg taken once per day in adults with overweight or obesity (OASIS 1): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet. 2023 Aug 26;402(10403):705-719. doi: 10.1016/S0140-6736(23)01185-6. Epub 2023 Jun 26.
- Wharton S, Konig M. GLP-1 Receptor Agonist Orforglipron for Adults with Obesity. Reply.
N Engl J Med. 2023 Dec 14;389(24):2304-2305. doi: 10.1056/NEJMc2311840.
- Sean Wharton, M.D., Thomas Blevins, M.D., et al. Daily Oral GLP-1 Receptor Agonist Orforglipron for Adults with Obesity. N Engl J Med 2023;389:877-88. DOI: 10.1056/NEJMoa2302392